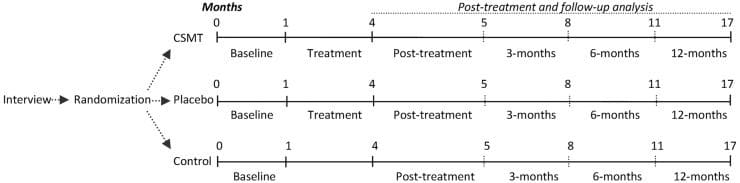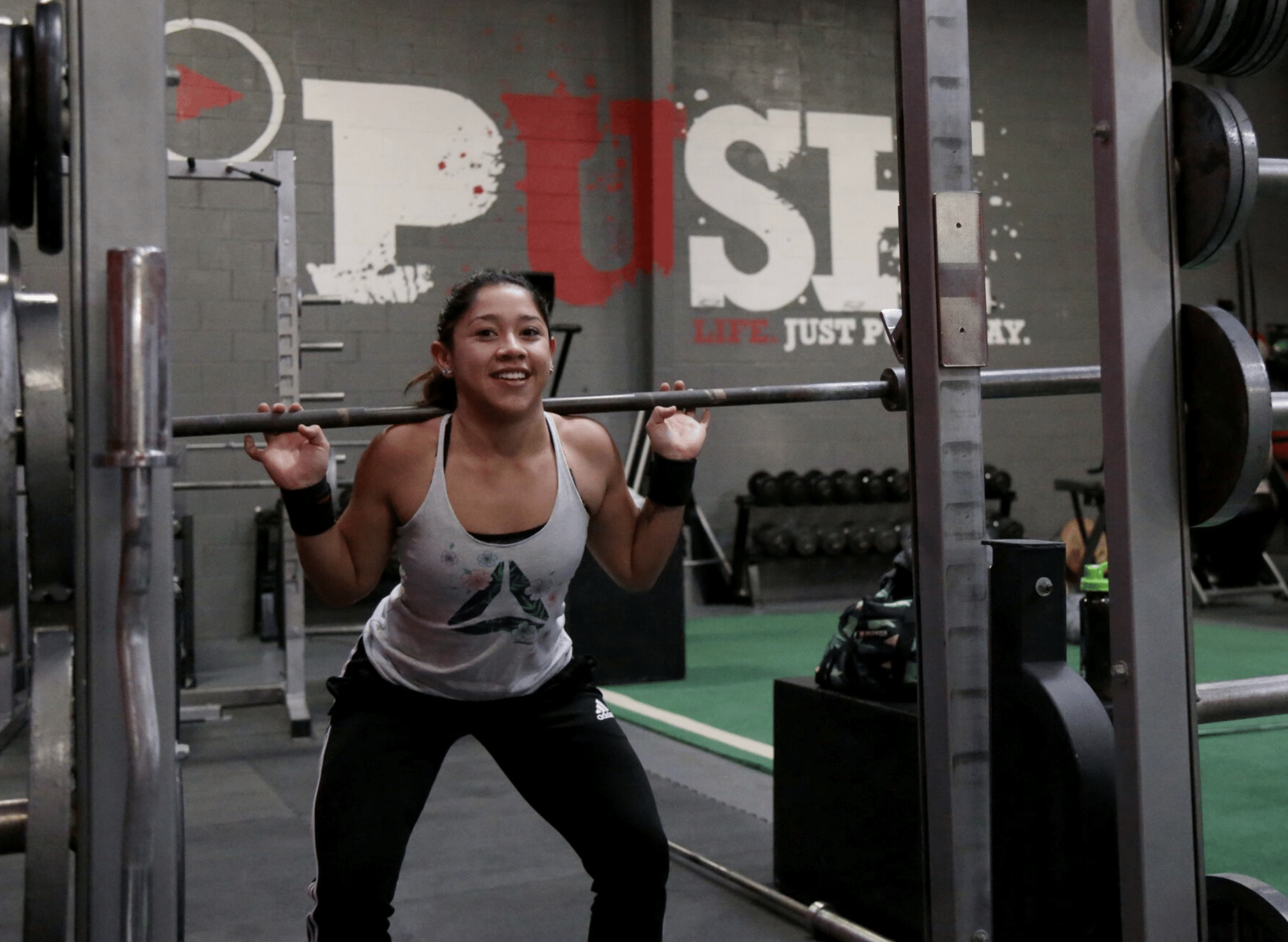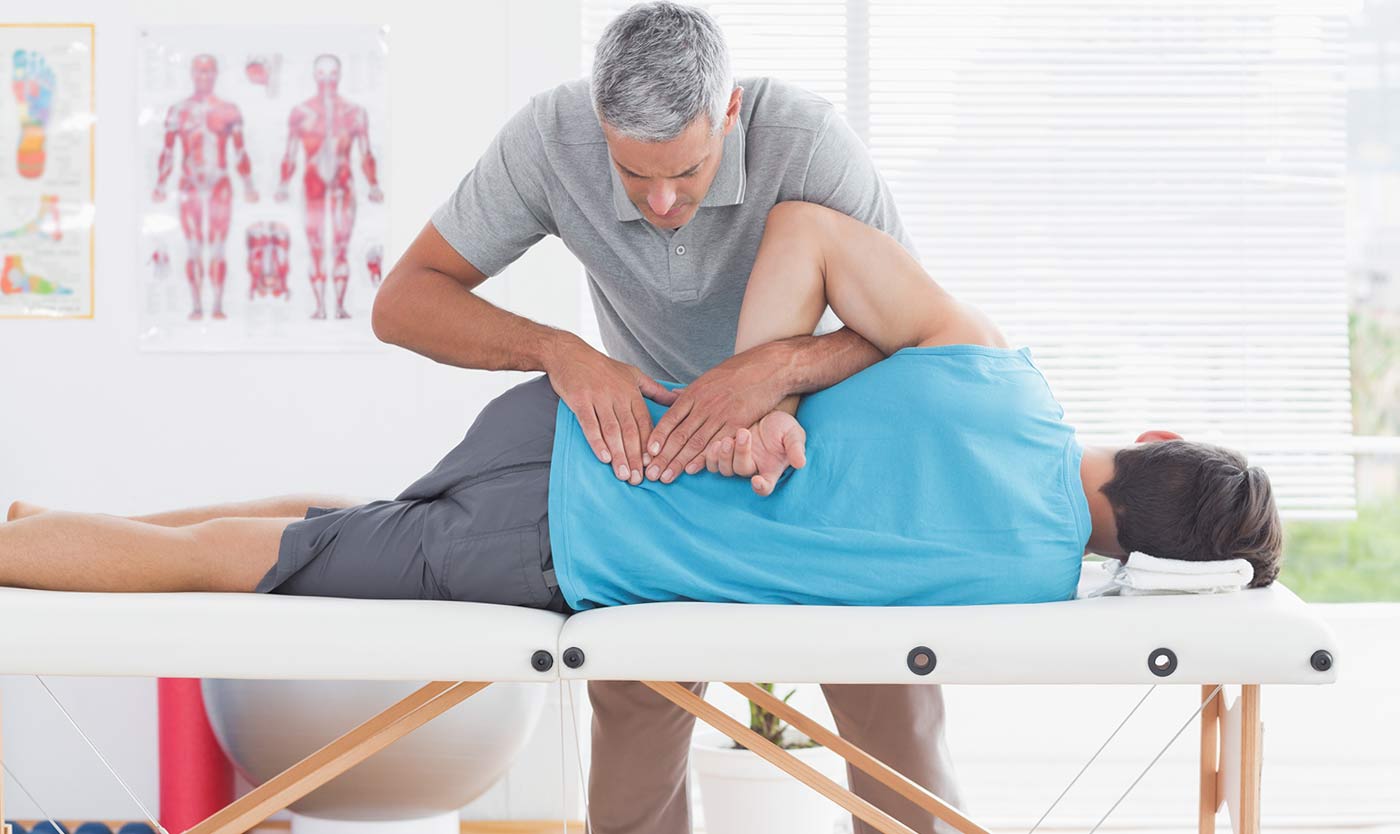
Лечение головной боли мигрени: перестройка позвонков в Atlas
Несколько типов головных болей могут повлиять на обычного человека, и каждый может возникать из-за различных травм и / или состояний, однако головные боли мигрени часто могут иметь гораздо более сложную причину. Многие медицинские работники и многочисленные исследования, основанные на фактических данных, пришли к выводу, что подвывих в шее или смещение позвонков в шейном отделе позвоночника являются наиболее частой причиной мигреней. Мигрень характеризуется сильной головной болью, обычно поражающей одну сторону головы, сопровождающейся тошнотой и нарушением зрения. Мигрень изнуряет. Приведенная ниже информация описывает тематическое исследование, касающееся влияния перестройки атласных позвонков на пациентов с мигренью.
Влияние перенастройки позвонков Атласа у лиц с мигренью: экспериментальное экспериментальное исследование
Абстрактные
Введение. В тематическом исследовании мигрени симптомы головной боли значительно уменьшались с сопровождающим увеличением показателя внутричерепного соответствия после релаксации позвонков атласа. Это экспериментальное экспериментальное исследование проводилось после того, как одиннадцать неврологов диагностировали мигрень, чтобы определить, можно ли повторить результаты заболевания в начале исследования, четвертую неделю и восьмую неделю, после вмешательства Национальной ассоциации шейного отдела хиропрактики. Вторичные результаты состояли из показателей качества жизни, связанных с мигренью. Методы. После осмотра невропатологом добровольцы подписали формы согласия и завершили исходные результаты, связанные с мигренью. Наличие несогласованности атласа позволило включить исследование, позволяющее собирать исходные данные МРТ. Уход за хиропрактикой продолжался в течение восьми недель. Постиндустриальное повторное наблюдение произошло на четвертой и восьмой неделях, связанных с измерением результатов, связанных с мигренью. Результаты. Пять из одиннадцати субъектов показали увеличение первичного результата, внутричерепное соблюдение; однако среднее изменение не показало статистической значимости. Конец исследования означает изменения в оценках результатов, связанных с мигренью, вторичный результат, выявил клинически значимое улучшение симптомов с уменьшением дней головной боли. Обсуждение. Отсутствие надежного повышения соответствия может быть понято логарифмическим и динамическим характером внутричерепного гемодинамического и гидродинамического течения, позволяя отдельным компонентам, содержащим соблюдение, меняться, в то время как в целом это не так. Результаты исследования показывают, что вмешательство перестройки атласа может быть связано с уменьшением частоты мигрени и значительным улучшением качества жизни, что приводит к значительному снижению инвалидности, связанной с головной болью, как это наблюдается в этой когорте. Однако для подтверждения этих результатов необходимо провести дальнейшее исследование с помощью контроля. Регистрационный номер Clinicaltrials.gov - NCT01980927.
Введение
Было высказано предположение, что смещенный атласный позвонок создает деформацию спинного мозга, нарушая нейронный трафик ядер ствола головного мозга в продолговатом мозге, что затрудняет нормальную физиологию [1-4].
Целью процедуры коррекции атласа, разработанной Национальной ассоциацией хиропрактики верхнего отдела шейки матки (NUCCA), является восстановление смещенных структур позвоночника по вертикальной оси или линии тяжести. Реконструкция, описываемая как `` принцип восстановления '', направлена на восстановление нормального биомеханического отношения верхнего шейного отдела позвоночника пациента к вертикальной оси (линии тяжести). Реставрация характеризуется как архитектурно сбалансированная, способная к неограниченному диапазону движений и позволяющая значительно снизить гравитационное напряжение [3]. Коррекция теоретически устраняет деформацию пуповины, вызванную смещением атласа или комплексом подвывиха атласа (ASC), в соответствии с определением NUCCA. Неврологическая функция восстанавливается, в частности, в вегетативных ядрах ствола головного мозга, которые влияют на сосудистую систему черепа, включая спинномозговую жидкость (CSF) [3, 4].
Интракраниальный индекс соответствия (ICCI), по-видимому, является более чувствительной оценкой изменений, сделанных в отношении краниоспинальных биомеханических свойств у пациентов с симптомами, чем локальные гидродинамические параметры скоростей потока CSF и замещения шнура [5]. Основываясь на этой информации, ранее наблюдавшиеся зависимости повышенного внутричерепного соответствия к выраженному уменьшению симптомов мигрени после переориентации алата послужили стимулом для использования ICCI в качестве первичного результата исследования.
ICCI влияет на способность центральной нервной системы (ЦНС) вмещать физиологические колебания объема, которые происходят, тем самым избегая ишемии нижележащих неврологических структур [5, 6]. Состояние высокого внутричерепного соответствия позволяет любое увеличение объема в интратекальном пространстве ЦНС, не вызывая увеличения внутричерепного давления, которое происходит прежде всего при приеме артерий во время систолы [5, 6]. Отток происходит в положении лежа на спине через внутренние яремные вены или при вертикальном, через параспинальный или вторичный венозный дренаж. Это обширное венозное сплетение является безветренным и анастомотическим, позволяя крови течь в ретроградном направлении, в ЦНС через постуральные изменения [7, 8]. Венозный дренаж играет важную роль в регулировании внутричерепной системы жидкости [9]. Соответствие, как представляется, является функциональным и зависит от свободного выхода крови через эти экстракраниальные венозные дренажные пути [10].
Повреждение головы и шеи может создать ненормальную функцию спинного венозного сплетения, которое может нарушить дренирование позвоночного веноза, возможно, из-за вегетативной дисфункции, вторичной по отношению к ишемии спинного мозга [11]. Это уменьшает размещение флуктуаций объема в черепе, создавая состояние снижения внутричерепного соответствия.
Damadian и Chu описывают возвращение нормального оттока CSF, измеренного в середине C-2, с уменьшением 28.6% измеренного градиента давления CSF у пациента, где атлас был оптимально перестроен [12]. Пациент сообщил о свободе от симптомов (головокружение и рвота при лежании) в соответствии с атласом, остающимся в расстановке.
Исследование артериальной гипертензии с использованием вмешательства NUCCA предполагает, что возможный механизм, лежащий в основе снижения артериального давления, может быть результатом изменений в мозговом кровообращении в зависимости от положения атлантических позвонков [13]. Кумада и др. исследовали тройнично-сосудистый механизм контроля артериального давления в стволе головного мозга [14, 15]. Goadsby et al. представили убедительные доказательства того, что мигрень возникает через тройнично-сосудистую систему, опосредованную стволом головного мозга и верхним шейным отделом позвоночника [16]. Эмпирическое наблюдение выявляет значительное снижение инвалидности мигрени у пациентов с головной болью после применения коррекции атласа. Использование субъектов с диагнозом мигрень казалось идеальным для исследования предполагаемых изменений мозгового кровообращения после перестройки атласа, как первоначально предполагалось в выводах исследования гипертонии и, казалось бы, подтверждается возможной связью ствола мозга и тройничного нерва с сосудом. Это будет способствовать дальнейшему развитию работающей патофизиологической гипотезы смещения атласа.
Результаты первоначального исследования показали значительное увеличение ICCI с уменьшением симптомов головной боли мигрени после коррекции атласа NUCCA. 62-летний мужчина с невропатологом диагностировал хроническую мигрень, добровольно вызванную до начала исследования. Используя фазовый контраст-МРТ (ПК-МРТ), изменения в параметрах церебрального гемодинамики и гидродинамического потока измерялись на начальном этапе, в течение 72, а затем через четыре недели после вмешательства атласа. Была проведена та же самая процедура коррекции атласа, которая использовалась в исследовании гипертензии [13]. Через 72 после исследования было обнаружено примечательное изменение индекса внутричерепного соответствия (ICCI), от 9.4 до 11.5, до 17.5 на четвертую неделю после вмешательства. Наблюдаемые изменения пульсации венозного оттока и преобладающего вторичного венозного дренажа в положении лежа на спине гарантировали дополнительное исследование, еще более вдохновляющее изучение предметов мигрени в этом случае.
Возможные последствия несоосности атласа или ASC при венозном дренировании неизвестны. Тщательный осмотр внутричерепного соответствия в отношении воздействия вмешательства несоосности атласа может дать представление о том, как коррекция может повлиять на головную боль мигрени.
Используя PC-MRI, основная цель этого текущего исследования и первичный результат, измеренные ICCI изменяются от базового уровня до четырех и восьми недель после вмешательства NUCCA в когорте неврологов, выбранных мигренями. Как отмечалось в случае исследования, гипотеза предполагала, что ICCI субъекта будет увеличиваться после вмешательства NUCCA с соответствующим уменьшением симптомов мигрени. Если они присутствуют, любые наблюдаемые изменения венозной пульсации и пути дренажа должны быть задокументированы для дальнейшего сравнения. Для мониторинга симптомов симптомов мигрени вторичные результаты включали результаты, полученные от пациентов, для измерения любых связанных с этим изменений в качестве качества жизни (HRQoL), аналогично используемых при исследовании мигрени. На протяжении всего исследования субъекты поддерживали дневники головной боли, документирующие уменьшение (или увеличение) количества дней головной боли, интенсивности и используемых лекарств.
Проведение этой серии наблюдений, экспериментальное исследование, позволило дополнительно исследовать вышеупомянутые физиологические эффекты при дальнейшем развитии рабочей гипотезы в патофизиологии несоосности атласа. Данные, необходимые для оценки статистически значимых размеров выборки субъектов и решения процедурных проблем, предоставят необходимую информацию для разработки уточненного протокола для проведения слепого плацебо-контролируемого исследования мигрени с использованием коррекционной коррекции NUCCA.
методы
Это исследование соответствовало Хельсинкской декларации в отношении исследований на людях. Объединенный совет по этике медицинских исследований Университета Калгари и Альберты при медицинском обслуживании утвердил протокол исследования и форму информированного согласия субъектов, идентификатор этики: E-24116. ClinicalTrials.gov присвоил номер NCT01980927 после регистрации этого исследования (Clinictrials.gov/ct2/show/NCT01980927).
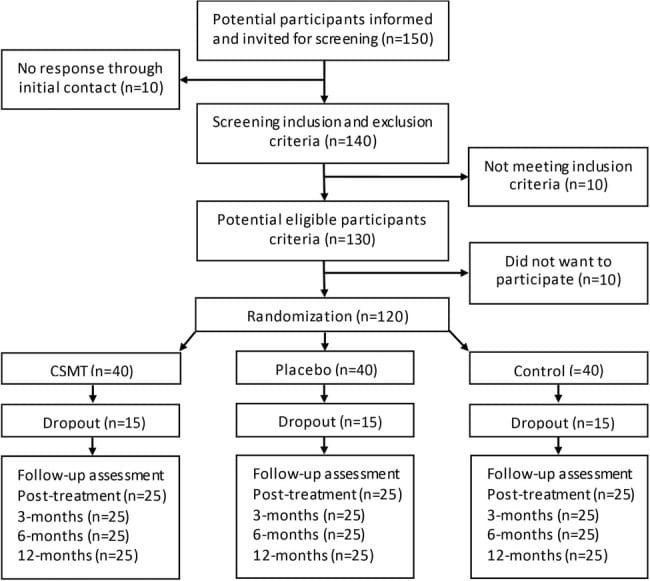
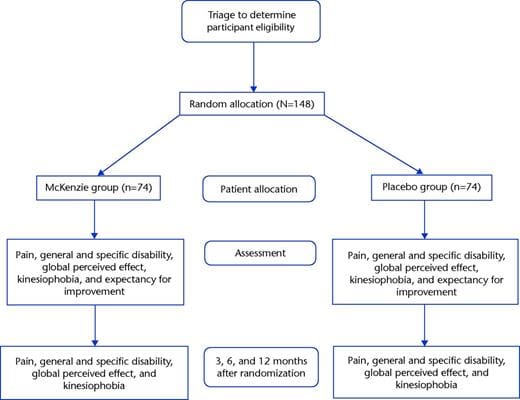
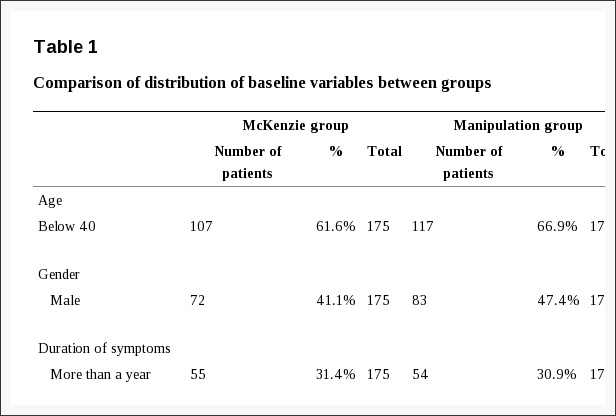
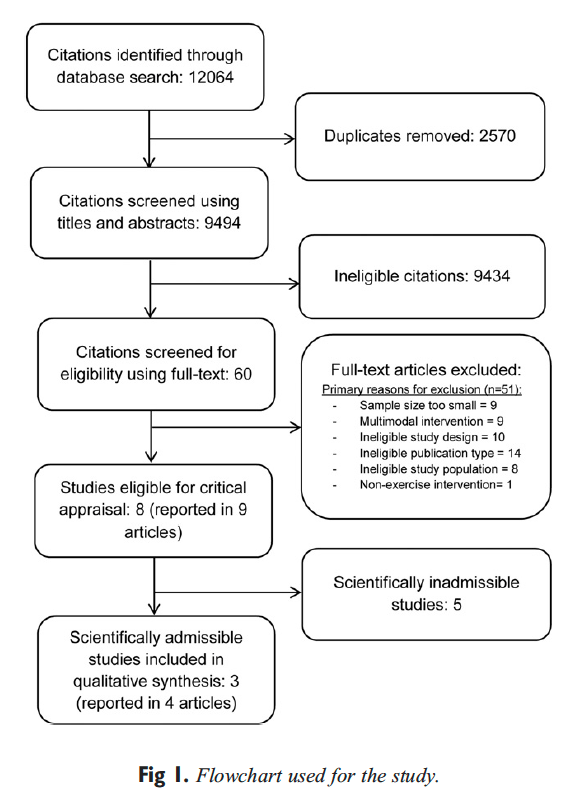
Подбор и скрининг субъектов проводились в программе оценки и управления головной болью в Калгари (CHAMP), специализированной специализированной клинике для специалистов по неврологии (см. Рисунок 1, таблица 1). CHAMP оценивает пациентов, устойчивых к стандартной фармакотерапии и лечению от головной боли мигрени, которая больше не обеспечивает облегчение симптомов мигрени. Врач из семейной и первичной медико-санитарной помощи передал потенциальные предметы исследования CHAMP, делая рекламу ненужной.
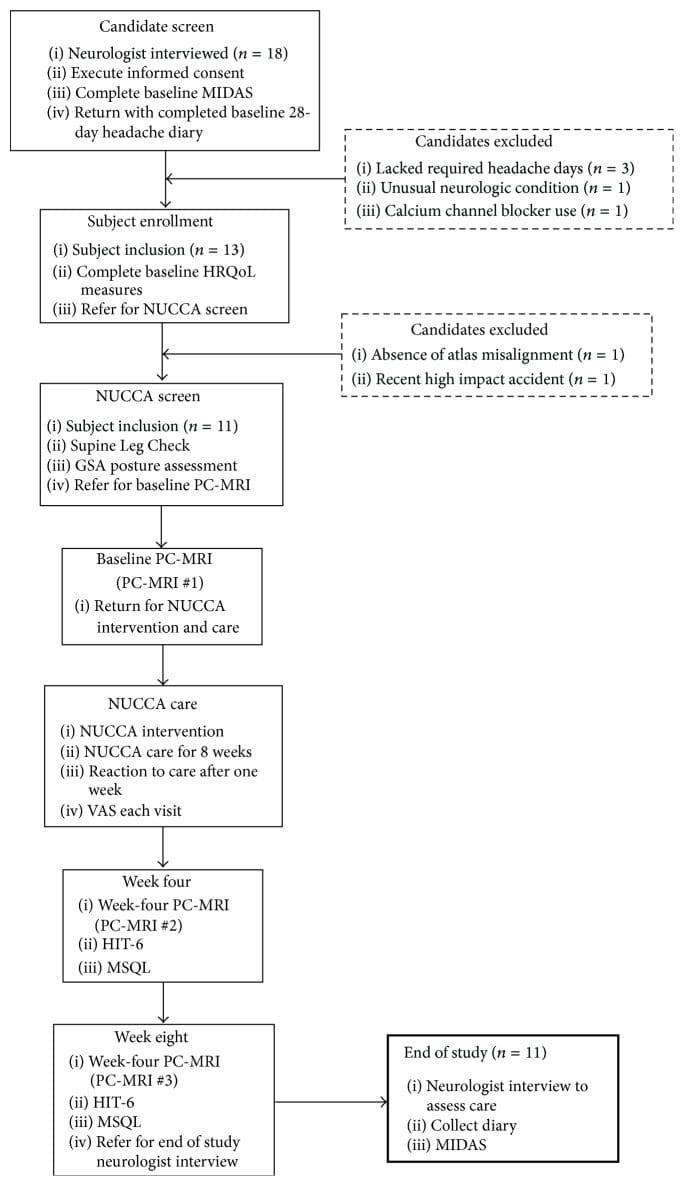
Рисунок 1: Распределение объектов и исследование (n = 11). GSA: Анализатор стресса для гравитации. HIT-6: Испытание на удар головной боли - 6. HRQoL: Качество жизни, связанное со здоровьем. MIDAS: шкала оценки инвалидности мигрени. MSQL: показатель качества жизни, характерный для мигрени. NUCCA: Национальная ассоциация хиропрактики шейного отдела. PC-MRI: визуализация магнитного резонанса с контрастностью фаз. VAS: визуальная аналоговая шкала.

Таблица 1: Критерии включения / исключения субъектов. Потенциальные пациенты, ранее не обращавшиеся к хиропрактикам верхних отделов шейки матки, демонстрировали от десяти до двадцати шести дней с головной болью в месяц, о которых они сообщали сами, за предыдущие четыре месяца. Требовалось не менее восьми дней с головной болью в месяц, интенсивность которых достигала не менее четырех по шкале боли от нуля до десяти по визуальной аналоговой шкале (ВАШ).
Для включения в исследование требовались добровольцы в возрасте от 21 до 65 лет, которые удовлетворяли определенным диагностическим критериям мигрени. Невролог с опытом работы в области мигрени в течение нескольких десятилетий проводил отбор кандидатов с использованием Международной классификации головных болей (ICHD-2) для включения в исследование [20]. Потенциальные субъекты, ранее не обращавшиеся к хиропрактике верхних отделов шейки матки, должны были продемонстрировать посредством самоотчета от десяти до двадцати шести дней с головной болью в месяц в течение предыдущих четырех месяцев. По крайней мере, восемь дней с головной болью в месяц должны были достигнуть интенсивности не менее четырех по шкале боли от нуля до десяти по ВАШ, если только лечение не было успешным с помощью лекарств, специфичных для мигрени. Требовалось по крайней мере четыре отдельных эпизода головной боли в месяц, разделенные по крайней мере 24-часовым безболезненным интервалом.
Значительная травма головы или шеи, возникающая в течение одного года до вступления в исследование, исключала кандидатов. К числу дополнительных критериев исключения относятся чрезмерное употребление острых лекарств, история клаустрофобии, сердечно-сосудистых или цереброваскулярных заболеваний или любое расстройство ЦНС, отличное от мигрени. В таблице 1 описаны все критерии включения и исключения. Используя опытного сертифицированного врача-невролога для скрининга потенциальных субъектов, придерживаясь ICHD-2 и руководствуясь критериями включения / исключения, исключение субъектов с другими источниками головной боли, таких как мышечное напряжение и лекарство, чрезмерная головная боль, приведет к увеличению вероятности успешной предметный набор.
Участники, отвечающие первоначальным критериям, подписали информированное согласие, а затем завершили базовую шкалу оценки инвалидности мигрени (MIDAS). MIDAS требует двенадцать недель, чтобы продемонстрировать клинически значимые изменения [21]. Это позволило пройти достаточно времени, чтобы выявить любые возможные изменения. В течение следующих дней 28 кандидаты записывали дневник головной боли, предоставляя базовые данные, подтверждая количество дней головной боли и интенсивность, необходимые для включения. После четырех недель диагностическое обоснование проверки дневника позволило администрировать оставшиеся базовые показатели HRQoL:
- Показатель качества жизни, характерный для мигрени (MSQL) [22],
- Тест на удар головной боли - 6 (HIT-6) [23],
- Тема текущей глобальной оценки боли в головной боли (VAS).
Направление к практикующему специалисту NUCCA для определения наличия смещения атласа подтвердило необходимость вмешательства, завершающего включение или исключение субъекта из исследования. Отсутствие индикаторов несовпадения атласа исключенных кандидатов. После записи на прием для вмешательства и ухода в NUCCA, квалифицированные субъекты прошли базовые измерения ПК-МРТ. Рисунок 1 суммирует расположение субъектов на протяжении всего исследования.
Первоначальное вмешательство NUCCA потребовало трех последовательных посещений: (1) День первый, оценка смещения атласа, рентгенограммы до коррекции; (2) День второй, коррекция NUCCA с оценкой после коррекции с помощью рентгенограмм; и (3) День третий, повторная оценка после исправления. Последующее наблюдение осуществлялось еженедельно в течение четырех недель, затем каждые две недели в течение оставшейся части периода исследования. При каждом посещении NUCCA субъекты выполняли текущую оценку головной боли (пожалуйста, оцените вашу головную боль в среднем за последнюю неделю), используя линейку и карандаш, отмечая линию 100 мм (ВАШ). Через неделю после первоначального вмешательства субъекты заполнили анкету «Возможная реакция на лечение». Эта оценка в прошлом использовалась для успешного мониторинга побочных эффектов, связанных с различными процедурами коррекции верхнего отдела шейки матки [24].
На четвертой неделе были получены данные PC-MRI, и испытуемые завершили MSQL и HIT-6. Окончание исследования PC-МРТ-данных было собрано на восьмой неделе, после чего было проведено интервью с неврологом. Здесь были собраны предметы, прошедшие окончательные результаты MSQOL, HIT-6, MIDAS и VAS и дневники головной боли.
На недельном посещении невролога 8 двум пациентам была предложена долгосрочная возможность наблюдения за весь период исследования в течение 24 недель. Это включало повторную оценку NUCCA ежемесячно в течение 16 недель после завершения начального исследования 8-week. Цель этой последующей деятельности заключалась в том, чтобы помочь определить, улучшилось ли улучшение головной боли при поддержании выравнивания атласа, наблюдая за любым долгосрочным эффектом ухода NUCCA в ICCI. Субъекты, желающие участвовать, подписали второе информированное согласие на этот этап обучения и продолжали ежемесячную помощь NUCCA. В конце 24 недель от первоначального вмешательства атласа произошло четвертое исследование изображений с использованием ПК-МРТ. На собеседовании с невропатологом были собраны итоговые результаты MSQOL, HIT-6, MIDAS, VAS и дневники головной боли.
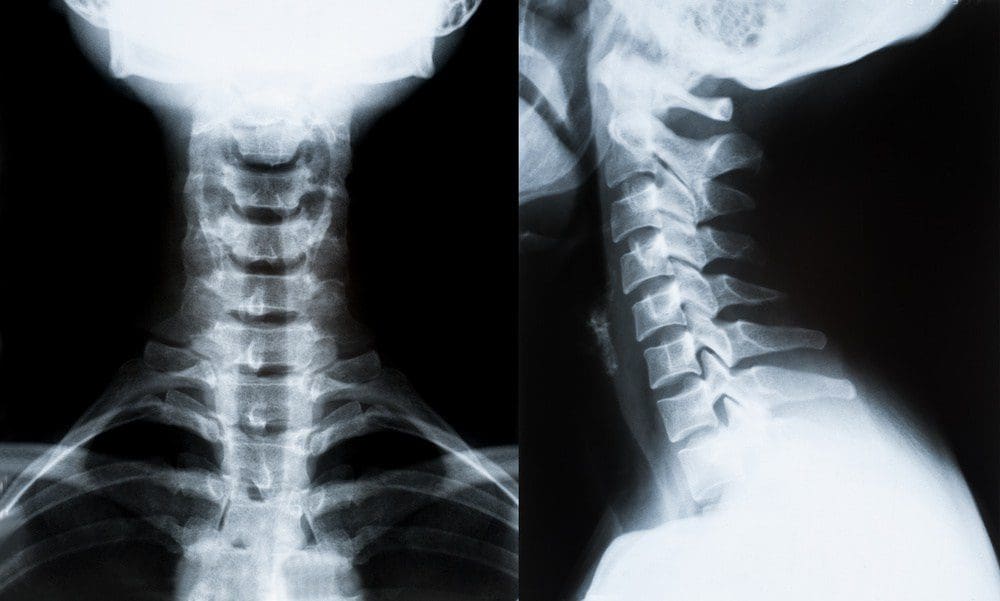
Та же процедура NUCCA, о которой сообщалось ранее, выполнялась с использованием установленного протокола и стандартов ухода, разработанных в рамках сертификации NUCCA для оценки и корректировки атласа или коррекции ASC (см. Рисунки 22-5) [2, 13, 25]. Оценка для ASC включает в себя скрининг на функциональное неравенство длины ног с помощью проверки на положение лежа на спине (SLC) и исследование постуральной симметрии с помощью анализатора гравитационного стресса (Upper Cervical Store, Inc., 1641 17 Avenue, Campbell River, BC, Canada V9W 4L5 ) (см. рисунки? Рисунки 22 и 3 (а) 3 (в)) [26 28]. Если обнаружены SLC и постуральный дисбаланс, показано трехкратное рентгенографическое исследование для определения многомерной ориентации и степени краниоцервикального смещения [29, 30]. Тщательный рентгенологический анализ дает информацию для определения оптимальной стратегии коррекции атласа для конкретного пациента. Врач находит анатомические ориентиры из серии с тремя проекциями, измеряя структурные и функциональные углы, которые отклоняются от установленных ортогональных стандартов. Затем степень смещения и ориентации атласа выявляются в трех измерениях (см. Рисунки 4 (а) - 4 (в)) [2, 29, 30]. Юстировка радиографического оборудования, уменьшение размера порта коллиматора, комбинации высокоскоростных пленок и экранов, специальные фильтры, специализированные сетки и свинцовая защита сводят к минимуму облучение объекта. Для этого исследования среднее общее измеренное входное воздействие на кожу у субъектов из серии рентгенографических исследований до и после коррекции составило 352 миллирада (3.52 миллизиверта).

Рисунок 2: Скрининговый тест с проверкой положения лежа на спине (SLC). Наблюдение очевидной «короткой ножки» указывает на возможное смещение атласа. Они даже кажутся.
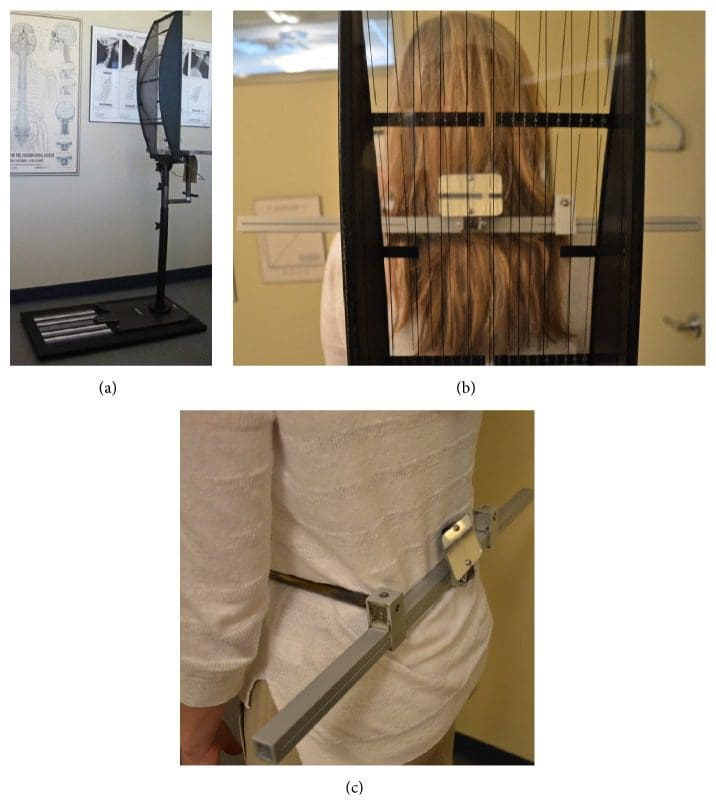
Рисунок 3: Анализатор стресса тяжести (GSA). (a) Устройство определяет постуральную асимметрию как дополнительный показатель несоосности атласа. Положительные результаты в SLC и GSA указывают на необходимость в радиографических сериях NUCCA. (б) Сбалансированный пациент без постуральной асимметрии. (c) Бедровые суппорты, используемые для измерения асимметрии таза.
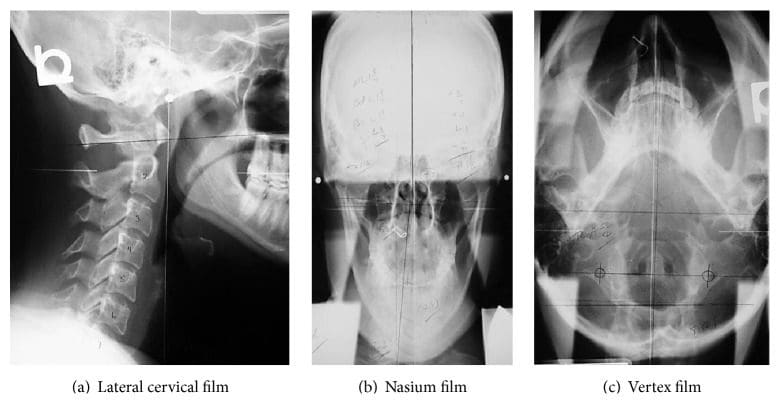
Рисунок 4: Серия радиограмм NUCCA. Эти пленки используются для определения несогласованности атласа и разработки стратегии коррекции. Послеоперационные рентгенограммы или постфильмы обеспечивают наилучшую коррекцию для этого объекта.
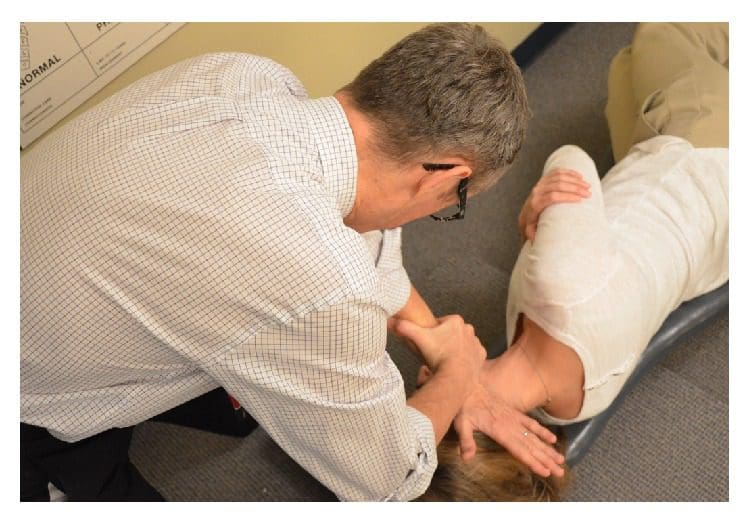
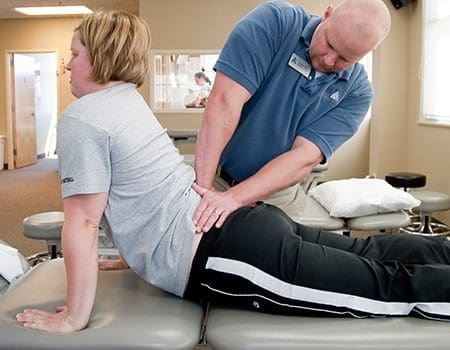
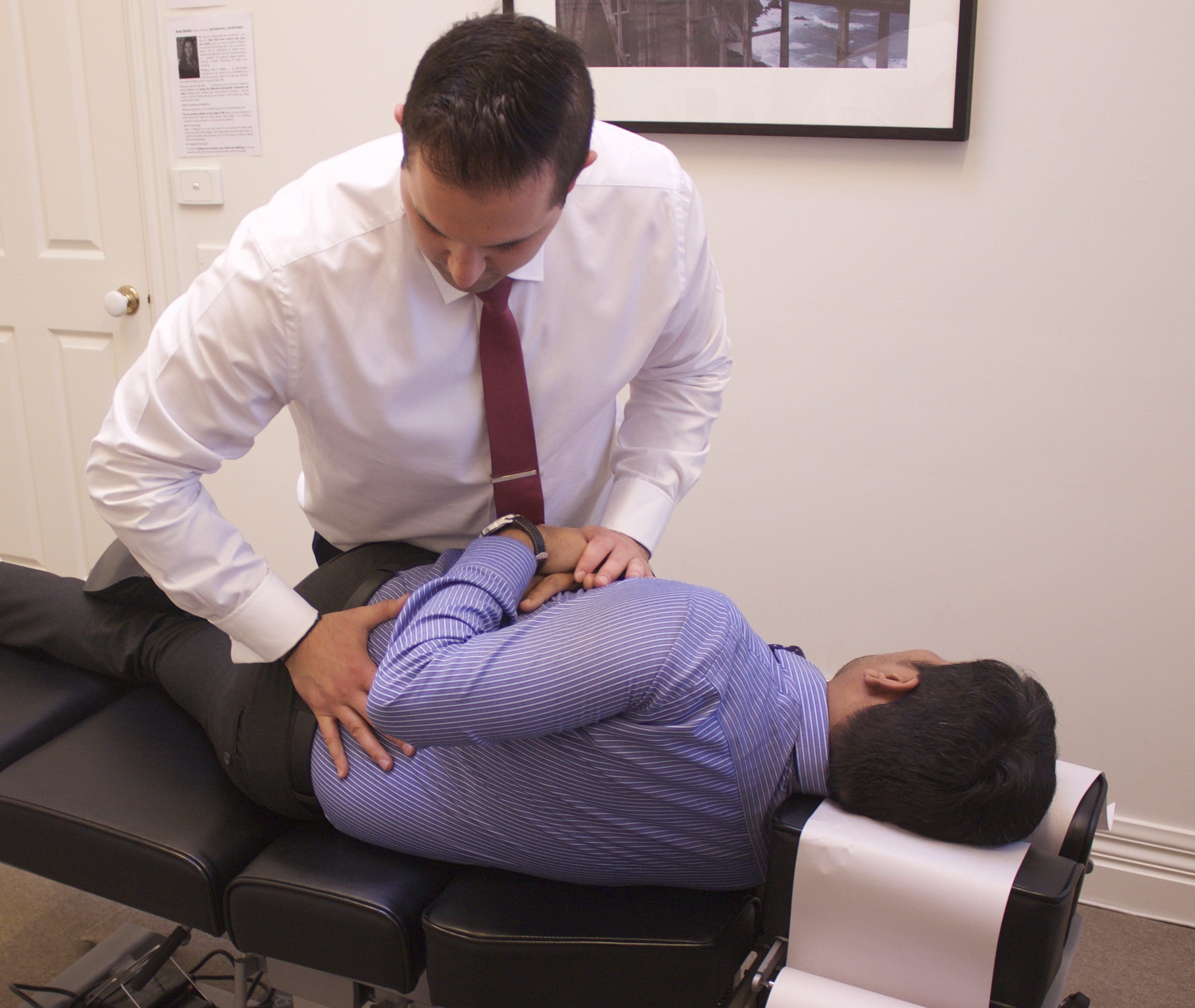
Рисунок 5: Выполнение коррекции NUCCA. Практикующий NUCCA обеспечивает регулировку тяги трицепса. Тело и руки практикующего выровнены, чтобы выполнить коррекцию атласа вдоль вектора оптимальной силы, используя информацию, полученную из рентгенограмм.
Вмешательство NUCCA включает в себя ручную коррекцию рентгенографически измеренного несоосности в анатомической структуре между черепом, атласным позвонком и шейным отделом позвоночника. Используя биомеханические принципы, основанные на рычажной системе, врач разрабатывает стратегию надлежащего
- позиционирование объекта,
- практикующая позиция,
- вектор силы, чтобы исправить несоосность атласа.
Предметы помещаются на столе боковой позы с головой, специально рамна с использованием сосцевидной системы поддержки. Применение заданного вектора управляемой силы для коррекции переводит череп в атлас и шею на вертикальную ось или центр тяжести позвоночника. Эти корректирующие силы контролируются по глубине, направлению, скорости и амплитуде, обеспечивая точное и точное уменьшение ASC.
Используя гороховидную кость контактной руки, врач NUCCA соприкасается с поперечным отростком атласа. Другая рука обхватывает запястье контактной руки, чтобы контролировать вектор, сохраняя при этом глубину силы, создаваемой при применении процедуры «тяги трехглавой мышцы» (см. Рисунок 5) [3]. Понимая биомеханику позвоночника, тело и руки практикующего выравниваются, чтобы произвести коррекцию атласа по оптимальному вектору силы. Контролируемая сила без толчков прилагается по заранее заданному пути сокращения. Он специфичен по своему направлению и глубине, чтобы оптимизировать сокращение ASC, гарантируя отсутствие активации реактивных сил мышц шеи в ответ на биомеханические изменения. Понятно, что оптимальное уменьшение смещения способствует долгосрочному сохранению и стабильности позвоночника.
После короткого периода отдыха выполняется процедура последующей оценки, идентичная первоначальной оценке. При проведении рентгенографического исследования после коррекции используется два вида для проверки возврата головы и шейного отдела позвоночника в оптимальный ортогональный баланс. Субъекты обучаются таким образом, чтобы сохранить их исправление, тем самым предотвращая другое несоосность.
Последующие посещения NUCCA состояли из дневных проверок головной боли и текущей оценки боли в головной боли (VAS). При определении необходимости другого вмешательства атласа использовалось неравномерность длины ног и чрезмерная постуральная асимметрия. Целью оптимального улучшения является то, что субъект будет поддерживать реорганизацию как можно дольше, при этом минимальное количество атласных вмешательств.
В PC-MRI-последовательности контрастные среды не используются. Методы PC-MRI собрали два набора данных с различной величиной чувствительности к потоку, полученной связыванием градиентных пар, которые последовательно дефазируют и перефазируют спины во время последовательности. Исходные данные из двух наборов вычитаются для расчета скорости потока.
Посещение физиологом МРТ на месте проводило обучение для технолога МРТ, и была установлена процедура передачи данных. Было проведено несколько сканирований практики и передачи данных, чтобы обеспечить сбор данных без проблем. В образовании и сборе данных использовался рентгеновский сканер 1.5-tesla GE 360 Optima MR (Milwaukee, WI) в центре обработки изображений (EFW Radiology, Калгари, Альберта, Канада). В анатомических сканировании использовалась фазовая решетка с фазированной решеткой 12, последовательная градиентная эхо-последовательность (MP-RAGE), полученная на основе намагниченности 3D. Данные, чувствительные к потоку, были получены с использованием метода параллельного приема (iPAT), коэффициента ускорения 2.
Чтобы измерить кровоток к основанию черепа и от него, были выполнены два ретроспективно стробированных, скоростно-кодированных сканирования фазового контраста в кинематографическом режиме, как определено по индивидуальной частоте сердечных сокращений, с получением тридцати двух изображений в течение сердечного цикла. Высокоскоростное кодирование (70 см / с) количественно определенное высокоскоростное кровоток, перпендикулярное сосудам на уровне C-2 позвонка, включает внутренние сонные артерии (ICA), позвоночные артерии (VA) и внутренние яремные вены (IJV). ). Данные вторичного венозного кровотока в позвоночных венах (VV), эпидуральных венах (EV) и глубоких шейных венах (DCV) были получены на одной и той же высоте с использованием последовательности низкоскоростного кодирования (7 см / с).
Тематические данные были идентифицированы по идентификатору исследования и дате исследования. Исследовательский нейрорадиолог проанализировал последовательности MR-RAGE, чтобы исключить патологические патологические состояния. Идентификаторы объекта были удалены и назначены кодированный идентификатор, разрешающий передачу по защищенному туннельному протоколу IP физику для анализа. Используя запатентованную программную объемную кровь, определяли формы волны потока цереброспинальной жидкости (CSF) и производные параметры (версия MRICP 1.4.35 Alinin Noninvasive Diagnostics, Miami, FL).
Используя сегментацию люменов на основе пульсаций, зависящие от времени объемные скорости потока рассчитывались путем интегрирования скоростей потока внутри областей просвета поперечного сечения по всем тридцати двум изображениям. Средние скорости потока были получены для цервикальных артерий, первичного венозного дренажа и вторичных путей венозного дренажа. Общий церебральный кровоток был получен путем суммирования этих средних скоростей потока.
Простое определение податливости - это соотношение изменений объема и давления. Внутричерепная податливость рассчитывается по соотношению максимального (систолического) изменения внутричерепного объема (ICVC) и колебаний давления во время сердечного цикла (PTP-PG). Изменение ICVC происходит из мгновенных различий между объемами крови и CSF, поступающих и выходящих из черепа [5, 31]. Изменение давления во время сердечного цикла выводится из изменения градиента давления в спинномозговой жидкости, который рассчитывается из МР-изображений потока спинномозговой жидкости с кодировкой скорости с использованием соотношения Навье-Стокса между производными скоростей и градиентом давления [5, 32 ]. Индекс внутричерепной податливости (ICCI) рассчитывается из соотношения ICVC и изменений давления [5, 31–33].
Статистический анализ рассмотрел несколько элементов. Анализ данных ICCI включал в себя один образец теста Колмогорова-Смирнова, показывающий отсутствие нормального распределения в данных ICCI, которые поэтому были описаны с использованием медианного и межквартильного диапазона (IQR). Различия между исходным уровнем и последующим наблюдением должны были быть изучены с использованием парного t-теста.
Данные оценки NUCCA были описаны с использованием среднего, медианного и межквартильного диапазона (IQR). Различия между исходным уровнем и последующим наблюдением были исследованы с использованием парного t-теста.
В зависимости от показателя результата, базового, недельного, восьминедельного и недельного (только MIDAS) последующие значения описывались с использованием среднего и стандартного отклонения. Данные MIDAS, собранные при первоначальном скрининге неврологов, имели один контрольный балл в конце двенадцати недель.
Отличия от базовой линии до каждого последующего визита были протестированы с использованием парного t-теста. Это привело к многочисленным значениям p из двух последующих посещений для каждого результата, за исключением MIDAS. Поскольку одна цель этого пилота заключается в предоставлении оценок для будущих исследований, важно описать, где были различия, а не использовать односторонний ANOVA для получения одного значения p для каждой меры. Забота о таких множественных сравнениях - увеличение частоты ошибок типа I.
Чтобы проанализировать данные VAS, оценки каждого предмета были рассмотрены индивидуально, а затем линейной регрессионной линией, которая адекватно соответствует данным. Использование многоуровневой модели регрессии с использованием как случайных перехватов, так и случайного наклона при условии, что для каждого пациента установлена индивидуальная линия регрессии. Это было проверено на случайной модели только для перехвата, которая соответствует линейной линии регрессии с общим наклоном для всех субъектов, в то время как условия перехвата могут меняться. Модель случайных коэффициентов была принята, поскольку не было доказательств того, что случайные наклоны значительно улучшают соответствие данных (используя статистическую статистику правдоподобия). Чтобы проиллюстрировать вариации перехватов, но не на склоне, отдельные линии регрессии были отображены для каждого пациента с наложенной средней регрессионной линией сверху.
Итоги
По результатам первоначального обследования неврологом, восемнадцать добровольцев соответствовали критериям включения. После заполнения дневников исходной головной боли пять кандидатов не соответствовали критериям включения. У трех не было необходимых дней с головной болью в дневниках исходного состояния, у одного были необычные неврологические симптомы с постоянным односторонним онемением, а у другого был прием блокатора кальциевых каналов. Практикующий NUCCA обнаружил, что два кандидата не соответствуют требованиям: у одного не было смещения атласа, а у второго - состояние Вольфа-Паркинсона-Уайта и серьезное искажение осанки (39 °), недавно имевшее место в тяжелой автомобильной аварии с сильным ударом и травмой позвоночника (см. Рис. .
Одиннадцать субъектов, восемь женщин и трое мужчин, средний возраст 21 год (диапазон 61 14.5 год), подходили для включения. Шесть субъектов страдали хронической мигренью, сообщая о пятнадцати или более днях с головной болью в месяц, при этом в среднем у одиннадцати субъектов головная боль была XNUMX дней в месяц. Продолжительность симптомов мигрени составляла от двух до тридцати пяти лет (в среднем двадцать три года). Все лекарства оставались неизменными на протяжении всего исследования, чтобы включить их схемы профилактики мигрени в соответствии с предписаниями.
По критериям исключения ни один из испытуемых не получал диагноз головной боли, связанный с травматическим повреждением головы и шеи, сотрясение мозга или постоянная головная боль, связанная с хлыстом. Девять испытуемых сообщили о очень далекой прошлой истории, более пяти лет и более (в среднем девять лет) до экрана невролога. Это включало связанные с спортом травмы головы, сотрясение мозга и / или хлыстовую травму. Два субъекта не указали на раннюю травму головы или шеи (см. Таблицу 2).
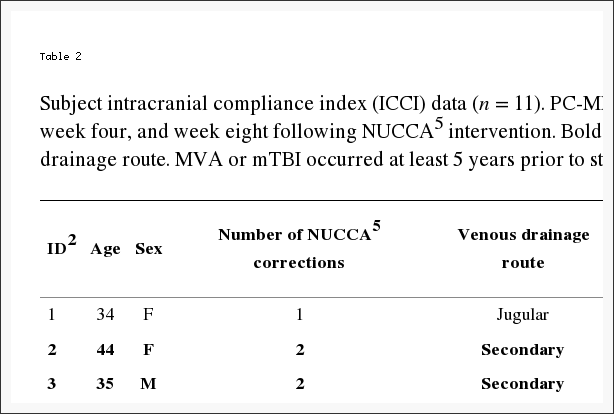
Таблица 2: Данные интракраниального индекса соответствия (ICCI) (n = 11). PC-MRI6 получил данные ICCI1, представленные на базовом уровне, четвертую неделю и восьмую неделю после вмешательства NUCCA5. Жирные ряды обозначают предмет с вторичным венозным дренажным путем. MVA или mTBI происходили по крайней мере за 5 лет до включения исследования, в среднем 10 лет.
По отдельности, пять субъектов продемонстрировали увеличение ICCI, значения трех субъектов остались практически такими же, а три показали снижение от исходного уровня до конца исследования. Общие изменения внутричерепной податливости показаны в Таблице 2 и на Рисунке 8. Медианные (IQR) значения ICCI составляли 5.6 (4.8, 5.9) на исходном уровне, 5.6 (4.9, 8.2) на четвертой неделе и 5.6 (4.6, 10.0) на 0.14-й неделе. неделя восьмая. Различия статистически не различались. Средняя разница между исходным уровнем и четвертой неделей составила? 95 (1.56% ДИ? 1.28, 0.834), p = 0.93, а между исходным уровнем и восьмой неделей составила 95 (0.99% ДИ? 2.84, 0.307), p = 24. Результаты 6-недельного исследования ICCI этих двух субъектов показаны в Таблице 01. Субъект 5.02 продемонстрировал тенденцию к увеличению ICCI с 6.69 на исходном уровне до 24 на 8 неделе, тогда как на 02 неделе результаты были интерпретированы как согласованные или оставшиеся неизменными. Субъект 15.17 продемонстрировал тенденцию к снижению ICCI от исходного уровня 9.47 до 24 на XNUMX неделе.
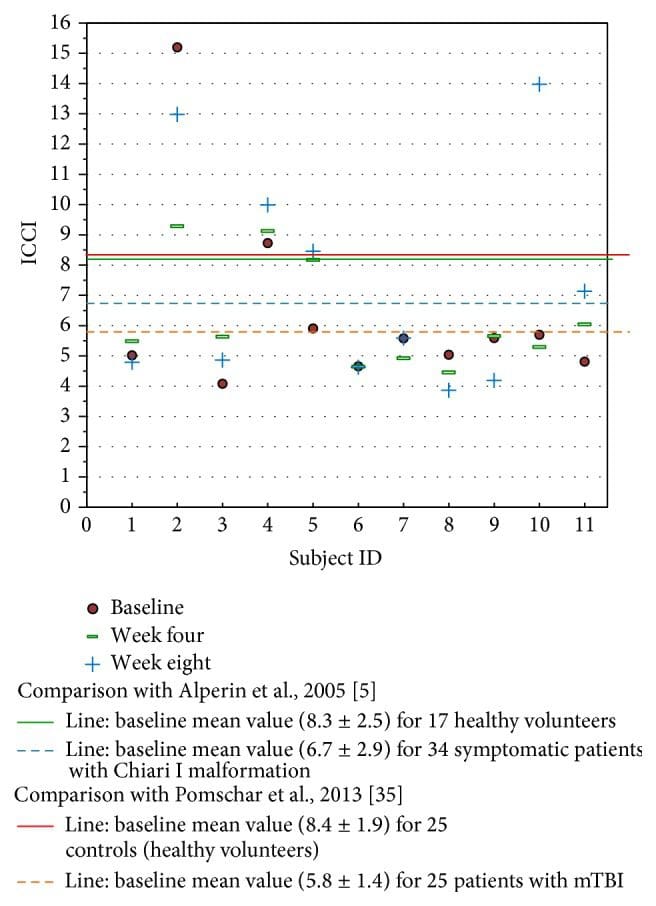
Рисунок 8: Изучите данные ICCI по сравнению с ранее сообщаемыми данными в литературе. Значения времени MRI фиксированы в начале, неделе 4 и неделе 8 после вмешательства. Исходные значения этого исследования совпадают с данными, полученными Pomschar по предметам, представленным только с mTBI.
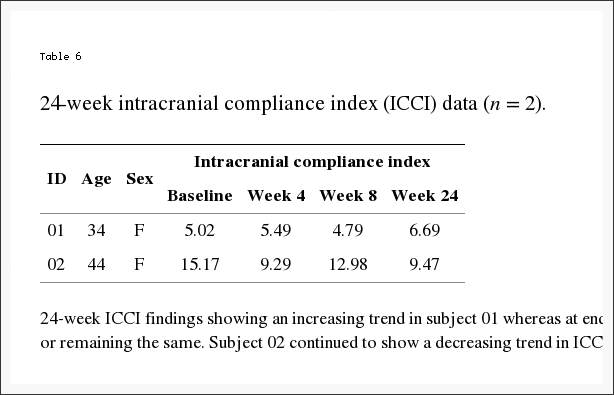
Таблица 6: 24-недельные результаты ICCI, показывающие возрастающую тенденцию к предмету 01, тогда как в конце исследования (неделя 8) результаты были интерпретированы как согласованные или остающиеся неизменными. Тема 02 продолжала демонстрировать тенденцию к снижению в ICCI.
В таблице 3 представлены изменения в оценках NUCCA. Средняя разница до и после вмешательства следующая: (1) SLC: 0.73 дюйма, 95% доверительный интервал (0.61, 0.84) (p <0.001); (2) GSA: 28.36 пункта шкалы, 95% ДИ (26.01, 30.72) (p <0.001); (3) Латеральность Атласа: 2.36 градуса, 95% ДИ (1.68, 3.05) (р <0.001); и (4) Вращение Атласа: 2.00 градуса, 95% ДИ (1.12, 2.88) (р <0.001). Это будет указывать на то, что после вмешательства атласа произошло вероятное изменение, основанное на оценке субъекта.
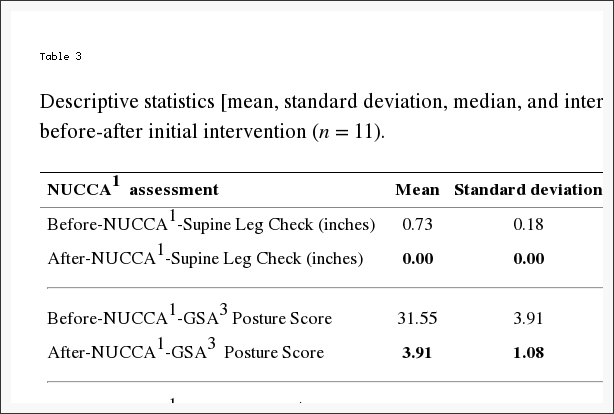
Таблица 3: Описательная статистика [среднее, стандартное отклонение, медианный и межквартильный диапазон (IQR2)] оценок NUCCA1 до-после начального вмешательства (n = 11).
Результаты дневника головной боли сообщаются в Таблица 4 и фигура 6. На исходном уровне у субъектов было в среднем 14.5 (SD = 5.7) дней с головной болью за 28 дней в месяц. В течение первого месяца после коррекции NUCCA среднее количество дней с головной болью в месяц уменьшилось на 3.1 дня по сравнению с исходным уровнем, 95% ДИ (0.19, 6.0), p = 0.039, до 11.4. В течение второго месяца количество дней с головной болью уменьшилось на 5.7 дней от исходного уровня, 95% ДИ (2.0, 9.4), p = 0.006, до 8.7 дней. На восьмой неделе у шести из одиннадцати пациентов количество дней с головной болью в месяц уменьшилось более чем на 30%. В течение 24 недель субъект 01 сообщил, что количество дней с головной болью практически не изменилось, в то время как у субъекта 02 наблюдалось уменьшение количества дней с головной болью на один день в месяц по сравнению с исходным уровнем исследования, равным семи, до шести дней в отчетах по окончании исследования.
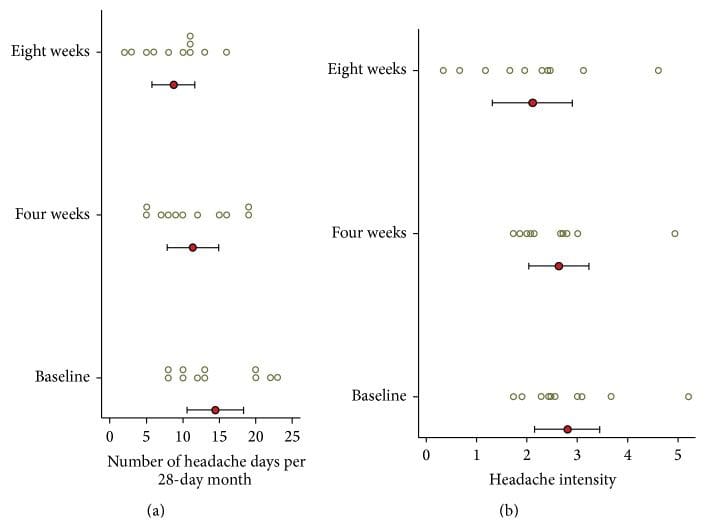
Рисунок 6: Головная боль и интенсивность боли в головной боли из дневника (n = 11). (a) Число дней головной боли в месяц. (b) Средняя интенсивность головной боли (в дни головной боли). Круг показывает среднее значение, а на панели отображается 95% CI. Круги - индивидуальные баллы. Значительное снижение дней головной боли в месяц отмечалось через четыре недели, почти в два раза в восемь недель. Четыре объекта (#4, 5, 7 и 8) показали снижение интенсивности головной боли более чем на 20%. Одновременное использование лекарств может объяснить небольшое снижение интенсивности головной боли.
На начальном этапе средняя интенсивность головной боли в дни с головной болью в масштабе от нуля до десяти составляла 2.8 (SD = 0.96). Средняя интенсивность головной боли не показала статистически значимого изменения у четырех (p = 0.604) и восьми (p = 0.158) недель. Четыре объекта (#4, 5, 7 и 8) показали снижение интенсивности головной боли более чем на 20%.
Показатели инвалидности в отношении качества жизни и головной боли приведены в таблице 4. Средний балл HIT-6 на базовой линии был 64.2 (SD = 3.8). На четвертой неделе после коррекции NUCCA среднее снижение баллов было 8.9, 95% CI (4.7, 13.1), p = 0.001. Показатели за неделю-восемь по сравнению с базовыми показателями показали среднее снижение по 10.4, 95% CI (6.8, 13.9), p = 0.001. В группе 24-недели тема 01 показала уменьшение 10 точек от 58 на неделе 8 до 48 на неделе 24, в то время как объект 02 уменьшил точки 7 от 55 на неделе 8 до 48 на неделе 24 (см. Рисунок 9).
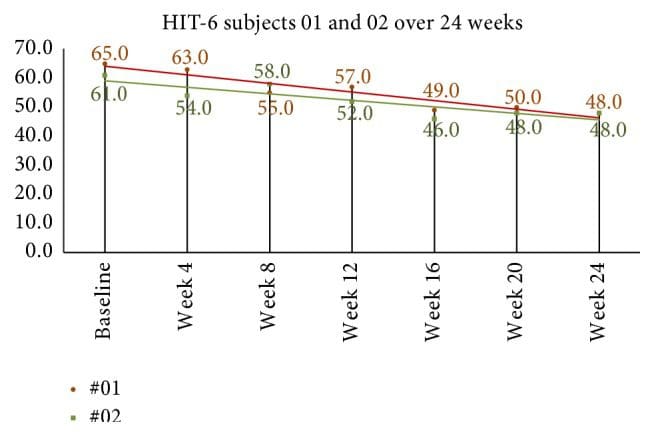
Рисунок 9: 24-недельные показатели HIT-6 в долгосрочных субъектах наблюдения. Месячные баллы продолжали снижаться после недели 8, конец первого исследования. На основе Smelt et al. критериев, можно интерпретировать, что минимально важное изменение в пределах человека произошло между неделей 8 и неделей 24. HIT-6: Испытание на удар головной боли - 6.
Средний исходный показатель MSQL составил 38.4 (SD = 17.4). На четвертой неделе после коррекции средние баллы для всех одиннадцати субъектов увеличились (улучшились) на 30.7, 95% ДИ (22.1, 39.2), p <0.001. К восьмой неделе, в конце исследования, средний балл MSQL увеличился по сравнению с исходным уровнем на 35.1, 95% ДИ (23.1, 50.0), p <0.001, до 73.5. Субъекты последующего наблюдения продолжали демонстрировать некоторое улучшение с увеличением баллов; тем не менее, многие показатели остались неизменными с 8 недели (см. рисунки 10 (a) - 10 (c)).
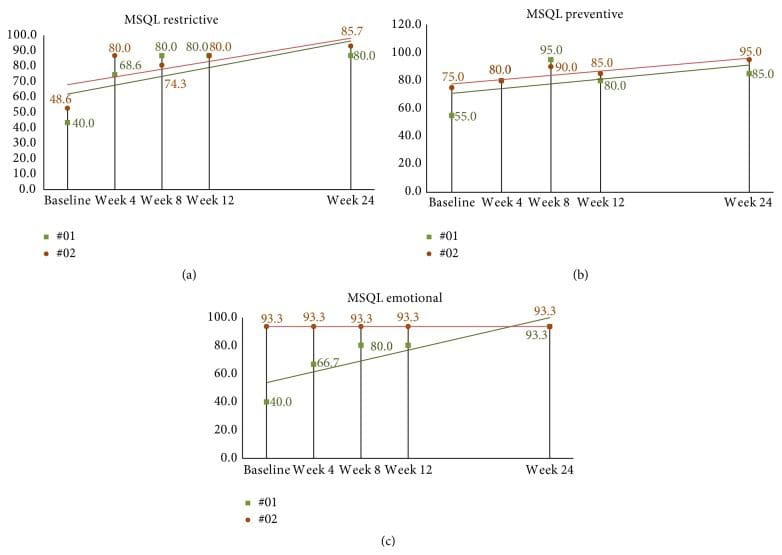
Рисунок 10: ((a) (c)) 24-недельные баллы MSQL у субъектов длительного наблюдения. (а) Субъект 01 практически вышел на плато после 8 недели до конца второго исследования. Субъект 02 показывает, что баллы увеличиваются с течением времени, демонстрируя минимально важные различия, основанные на Cole et al. к 24-й неделе. (b) Похоже, что к 8-й неделе оценки испытуемых достигают пика, при этом оба предмета показывают одинаковые баллы на 24-й неделе. (c) Показатели испытуемого 2 остаются неизменными на протяжении всего исследования, в то время как испытуемый 01 показывает устойчивое улучшение от исходного уровня до конца неделя 24. MSQL: Измерение качества жизни при мигрени.
Средний балл по MIDAS на исходном уровне составлял 46.7 (SD = 27.7). Через два месяца после коррекции NUCCA (через три месяца после исходного уровня) среднее снижение баллов по MIDAS у субъекта составило 32.1, 95% ДИ (13.2, 51.0), p = 0.004. Субъекты последующего наблюдения продолжали демонстрировать улучшение со снижением баллов при минимальном улучшении интенсивности (см. Рисунки 11 (a) - 11 (c)).
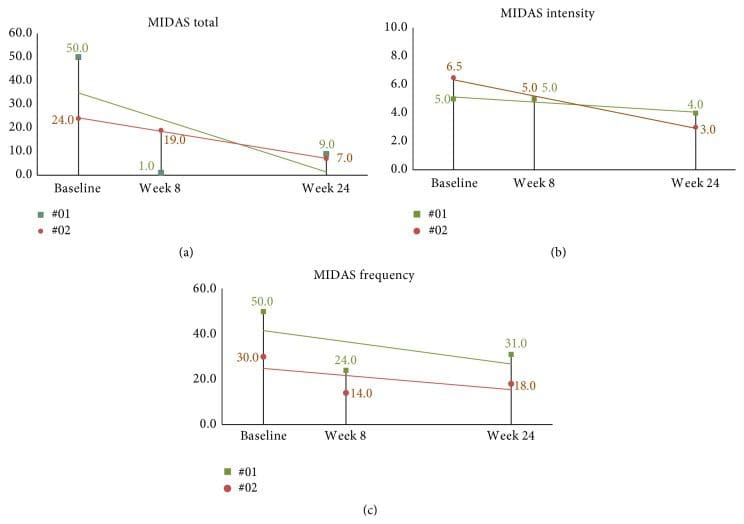
Рисунок 11: 24-неделя MIDAS оценивается в долгосрочных субъектах наблюдения. (a) Суммарные оценки MIDAS продолжали тенденцию к снижению в течение периода исследования 24 за неделю. (b) Показатели интенсивности продолжали улучшаться. (c) Хотя частота 24-недели была выше, чем на неделе 8, улучшение наблюдается по сравнению с базовым. MIDAS: шкала оценки инвалидности мигрени.
Оценка текущей головной боли по данным шкалы ВАШ представлена на рисунке 7. Модель многоуровневой линейной регрессии показала доказательства случайного эффекта для точки пересечения (p <0.001), но не для наклона (p = 0.916). Таким образом, принятая модель случайного пересечения оценивала разные точки пересечения для каждого пациента, но с общим наклоном. Расчетный наклон этой линии составил? 0.044, 95% ДИ (? 0.055,? 0.0326), p <0.001, что указывает на значительное снижение оценки по ВАШ на 0.44 за 10 дней после исходного уровня (p <0.001). Средний исходный балл составил 5.34, 95% ДИ (4.47, 6.22). Анализ случайных эффектов показал существенные различия в исходной оценке (SD = 1.09). Поскольку случайные перехваты обычно распределяются, это указывает на то, что 95% таких перехватов лежат между 3.16 и 7.52, что свидетельствует о существенных различиях в исходных значениях у пациентов. Показатели ВАШ продолжали улучшаться в группе наблюдения за двумя пациентами через 24 недели (см. Рисунок 12).
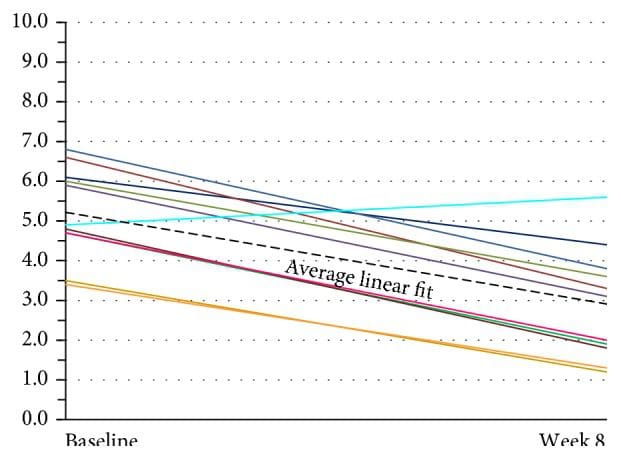
Рисунок 7: Тема глобальной оценки головной боли (VAS) (n = 11). Существенные различия в исходных показателях у этих пациентов. Линии показывают индивидуальную линейную пригодность для каждого из одиннадцати пациентов. Толстая пунктирная черная линия представляет собой среднюю линейную посадку для всех одиннадцати пациентов. VAS: визуальная аналоговая шкала.
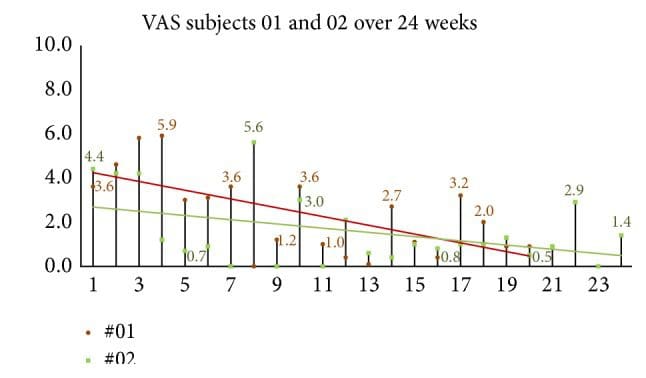
Рисунок 12: Глобальная оценка головной боли (ВАШ) в группе наблюдения в течение 24 недель. Когда испытуемых опрашивали, «пожалуйста, оцените вашу головную боль в среднем за последнюю неделю». Показатели ВАШ продолжали улучшаться в группе наблюдения с двумя участниками через 24 недели.
Наиболее очевидной реакцией на вмешательство и помощь NUCCA, о которых сообщили десять пациентов, был дискомфорт в мягкой шейке, в среднем оцениваемый в три из десяти баллов по оценке боли. У шести испытуемых боль начиналась более чем через двадцать четыре часа после коррекции атласа, длившейся более двадцати четырех часов. Ни один субъект не сообщил о каком-либо значительном влиянии на их повседневную деятельность. Все испытуемые сообщили об уходе за помощью NUCCA после одной недели, средний балл - десять, по шкале оценки от нуля до десяти.

Взгляд доктора Алекса Хименеса
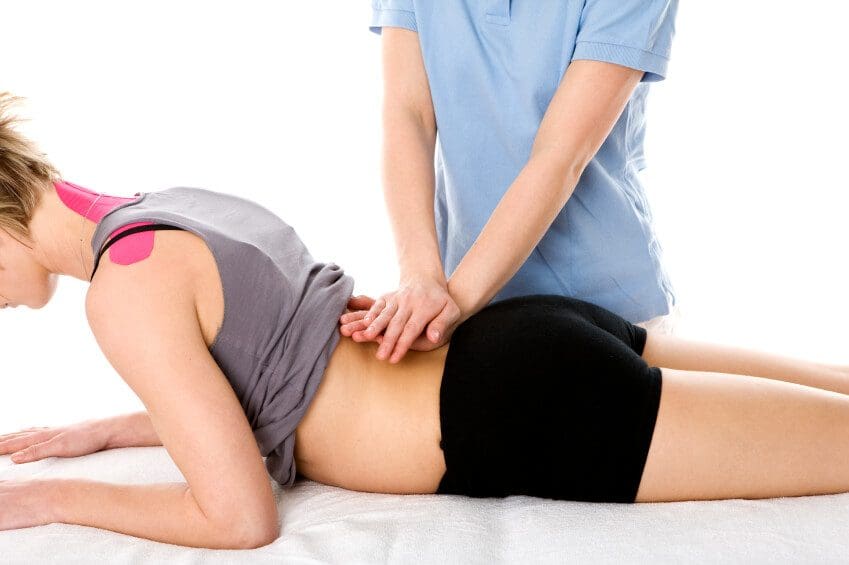
«Я уже несколько лет страдаю от мигрени. Есть ли причина головной боли? Что я могу сделать, чтобы уменьшить или избавиться от симптомов? » Головные боли мигрени, как полагают, являются сложной формой головной боли, однако причина для них такая же, как и у любого другого типа головной боли. Травматическая травма шейного отдела позвоночника, такая как хлыстовая травма от автомобильной аварии или спортивная травма, может привести к смещению в области шеи и верхней части спины, что может привести к мигрени. Неправильное положение также может вызывать проблемы с шеей, которые могут привести к боли в голове и шее. Специалист в области здравоохранения, специализирующийся на вопросах здоровья позвоночника, может диагностировать источник головной боли мигрени. Кроме того, квалифицированный и опытный специалист может выполнять коррекцию позвоночника, а также ручные манипуляции, чтобы помочь устранить любые несоосности позвоночника, которые могут вызывать симптомы. В следующей статье кратко излагается тематическое исследование, основанное на улучшении симптомов после релаксации позвонков атласа у участников мигрени.
Обсуждение
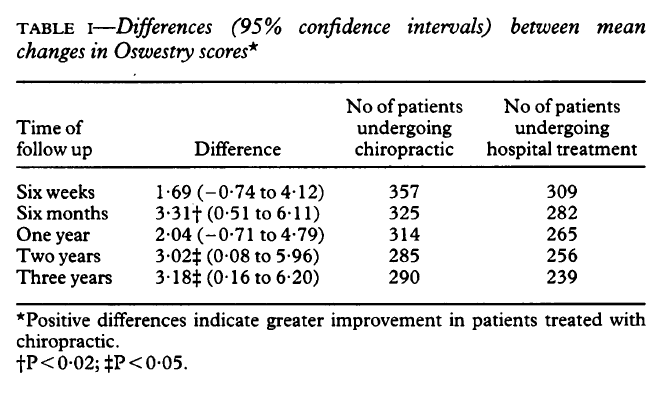
В этой ограниченной когорте из одиннадцати субъектов мигрени не было статистически значимых изменений в ICCI (первичный результат) после вмешательства NUCCA. Однако существенное изменение вторичных результатов HRQoL произошло, как показано в таблице 5. Согласованность в величине и направлении улучшения по этим показателям HRQoL указывает на уверенность в улучшении состояния головной боли в течение двухмесячного исследования после базового периода 28-дня.
Основываясь на результатах тематического исследования, это исследование предположило значительное увеличение ICCI после вмешательство в атлас который не наблюдался. Использование PC-MRI позволяет количественно определить динамическую взаимосвязь между притоком артерий, венозным оттоком и потоком CSF между черепом и спинальным каналом [33]. Интракраниальный индекс соответствия (ICCI) измеряет способность мозга реагировать на входящую артериальную кровь во время систолы. Интерпретация этого динамического потока представлена моноэкспоненциальной зависимостью, существующей между объемом CSF и давлением CSF. При увеличении или увеличении внутричерепного соответствия, также определяемом как хороший компенсационный резерв, входящая артериальная кровь может быть размещена внутричерепным содержимым с меньшим изменением внутричерепного давления. Хотя может произойти изменение внутричерепного объема или давления, исходя из экспоненциального характера отношения объем-давление, изменение ICCI после вмешательства может не быть реализовано. Расширенный анализ данных МРТ и дальнейшее исследование необходимы для определения практических количественных параметров для использования в качестве объективного результата, чувствительного для документирования физиологических изменений после коррекции атласа.
Koerte et al. отчеты пациентов с хронической мигренью демонстрируют значительно более высокий относительный вторичный венозный дренаж (параспинальное сплетение) в положении лежа на спине по сравнению с контрольными по возрасту и полу [34]. Четыре предмета исследования показали вторичный венозный дренаж с тремя из этих субъектов, демонстрирующий заметное увеличение соответствия после вмешательства. Значение неизвестно без дальнейшего изучения. Аналогично, Pomschar et al. сообщили, что субъекты с легкой травматической черепно-мозговой травмой (mTBI) демонстрируют повышенный дренаж через вторичный венозный параспинальный путь [35]. Средний показатель внутричерепного соответствия значительно ниже в когорте mTBI по сравнению с контрольными.
Некоторая перспектива может быть достигнута в сравнении данных ICCI этого исследования с ранее сообщенными нормальными субъектами, а также с mTBI, показанным на рисунке 8 [5, 35]. Ограниченное небольшим количеством изученных предметов, значимость этих результатов исследования может иметь отношение к Pomschar et al. остается неизвестным, предлагая только предположение о возможностях для будущих исследований. Это еще больше осложняется непоследовательным изменением ICCI, наблюдаемым у двух испытуемых, следующих за неделями 24. Второй предмет со вторичным рисунком дренажа показал уменьшение ICCI после вмешательства. Более крупное плацебо-контролируемое исследование со статистически значимым размером выборки субъекта могло бы продемонстрировать окончательное объективно измеренное физиологическое изменение после применения процедуры коррекции NUCCA.
Меры HRQoL используются клинически для оценки эффективности стратегии лечения для уменьшения боли и инвалидности, связанных с головной болью мигрени. Ожидается, что эффективное лечение улучшит восприятие пациентами боли и инвалидности, измеренное этими инструментами. Все показатели HRQoL в этом исследовании продемонстрировали значительное и значительное улучшение на четвертой неделе после вмешательства NUCCA. С четвертой недели до восьми были отмечены лишь незначительные улучшения. Опять же, только небольшие улучшения были отмечены у двух испытуемых, следующих за неделями 24. Хотя это исследование не предназначалось для демонстрации причинно-следственной связи от вмешательства NUCCA, результаты HRQoL создают непреходящий интерес для дальнейшего изучения.
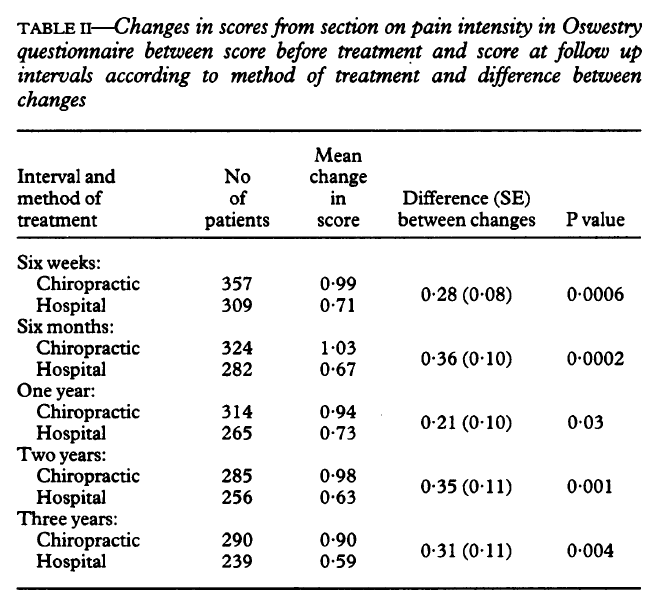
Из дневника с головной болью значительное снижение количества головных болей в месяц отмечалось через четыре недели, что почти удвоилось за восемь недель. Однако существенные различия в интенсивности головной боли во времени не были заметны из этих данных дневника (см. Рис. 5). В то время как число головных болей уменьшилось, субъекты все еще использовали медикаменты для поддержания интенсивности головной боли на допустимых уровнях; следовательно, предполагается, что статистически значимое различие в интенсивности головной боли не может быть определено. Последовательность в числах дней головной боли, происходящих на неделе 8 в последующих субъектах, может помочь будущему исследованию сосредоточиться на определении того, когда произойдет максимальное улучшение, чтобы помочь в установлении стандарта NUCCA по уходу за мигренью.
Клинически значимое изменение HIT-6 важно для полного понимания наблюдаемых результатов. Клинически значимое изменение для отдельного пациента определено в руководстве пользователя HIT-6 как? 5 [36]. Coeytaux et al., Используя четыре различных метода анализа, предполагают, что различие между группами в баллах HIT-6 в 2.3 единицы с течением времени может считаться клинически значимым [37]. Смелт и др. изучили популяции пациентов с мигренью первичной медико-санитарной помощи при разработке предлагаемых рекомендаций с использованием изменений баллов HIT-6 для клинической помощи и исследований [38]. В зависимости от последствий, возникающих в результате ложных срабатываний или отрицательных результатов, минимально важное изменение внутри человека (MIC) с использованием подхода «среднего изменения» было оценено в 2.5 балла. При использовании «анализа кривой рабочей характеристики приемника (ROC)» необходимо 6-точечное изменение. Рекомендуемая межгрупповая минимально важная разница (MID) - 1.5 [38].
Используя подход «среднего изменения», все испытуемые, кроме одного, сообщили об изменении (уменьшении) более чем на? 2.5. «Анализы РОС» также продемонстрировали улучшение у всех испытуемых, кроме одного. В каждом сравнительном анализе этот `` один испытуемый '' был другим человеком. На основании Smelt et al. По критериям, пациенты продолжали демонстрировать минимально важные улучшения, как показано на Рисунке 10.
Все испытуемые, кроме двух, показали улучшение показателей MIDAS между исходным уровнем и результатами через три месяца. Величина изменения была пропорциональна исходному баллу MIDAS, при этом все испытуемые, кроме трех, сообщили об общем изменении на пятьдесят процентов или больше. Субъекты последующего наблюдения продолжали демонстрировать улучшение, о чем свидетельствует продолжающееся снижение баллов к 24-й неделе; см. Рисунки 11 (a) - 11 (c).
Использование HIT-6 и MIDAS вместе в качестве клинического результата может обеспечить более полную оценку факторов инвалидности, связанных с головной болью [39]. Различия между двумя шкалами могут предсказывать инвалидность от интенсивности болей в головной боли и частоты головной боли, предоставляя дополнительную информацию о факторах, связанных с указанными изменениями, чем результат, использованный в одиночку. Хотя MIDAS, по-видимому, больше изменяется по частоте головной боли, интенсивность головной боли, по-видимому, влияет на показатель HIT-6 больше, чем MIDAS [39].
Как влияет головная боль мигрени и ограничивает ежедневное функционирование пациента, сообщается MSQL v. 2.1 в трех доменах 3: роль ограничительная (MSQL-R), ролевая профилактика (MSQL-P) и эмоциональное функционирование (MSQL-E). Увеличение баллов указывает на улучшение в этих областях со значениями от 0 (бедных) до 100 (лучше всего).
Оценка надежности шкал MSQL, проведенная Bagley et al. сообщают, что результаты должны быть от умеренной до сильной коррелированной с HIT-6 (r =? 0.60 до? 0.71) [40]. Исследование Cole et al. сообщает о клинических изменениях минимально важных различий (MID) для каждого домена: MSQL-R = 3.2, MSQL-P = 4.6 и MSQL-E = 7.5 [41]. Результаты исследования топирамата сообщают об индивидуальном минимально важном клиническом изменении (MIC): MSQL-R = 10.9, MSQL-P = 8.3 и MSQL-E = 12.2 [42].
Все испытуемые, кроме одного, испытывали индивидуальное минимально важное клиническое изменение для MSQL-R больше, чем 10.9, в течение восьми недель наблюдения в MSQL-R. Все, кроме двух субъектов, сообщили об изменениях, превышающих точки 12.2 в MSQL-E. Улучшение показателей MSQL-P увеличилось на десять пунктов и более по всем предметам.
Регрессионный анализ рейтингов ВАС с течением времени показал значительное линейное улучшение по сравнению с 3-месячным периодом. Существенные различия в исходных показателях у этих пациентов. Темпы улучшения не наблюдались. Эта тенденция, по-видимому, одинакова у испытуемых, изученных в течение 24 недель, как показано на рисунке 12.

Многие исследования с использованием фармацевтического вмешательства показали значительный эффект плацебо у пациентов из мигрирующих популяций [43]. Определение возможного улучшения мигрени в течение шести месяцев с использованием другого вмешательства, а также без вмешательства, важно для любого сравнения результатов. Исследование плацебо-эффектов обычно согласуется с тем, что вмешательства плацебо оказывают симптоматическое облегчение, но не изменяют патофизиологические процессы, лежащие в основе состояния [44]. Объективные МРТ-меры могут помочь выявить такой эффект плацебо, продемонстрировав изменение физиологических измерений параметров потока, возникающих после вмешательства плацебо.
Использование магнита с тремя теслами для сбора данных МРТ повысит надежность измерений за счет увеличения объема данных, используемых для расчета потока и ICCI. Это одно из первых исследований, использующих изменения в ICCI как результат оценки вмешательства. Это создает проблемы при интерпретации полученных МРТ данных для обоснования выводов или дальнейшего развития гипотезы. Сообщалось о изменчивости взаимосвязей между кровотоком в мозг, потоком CSF и частотой сердечных сокращений этих специфических для конкретного объекта параметров [45]. Вариации, наблюдаемые в небольшом трехтомном исследовании повторных мер, привели к выводам о том, что информацию, собранную из отдельных случаев, следует интерпретировать с осторожностью [46].
В литературе также сообщается в более крупных исследованиях о значительной надежности сбора этих данных объемного потока, полученных с помощью МРТ. Wentland et al. сообщили, что измерения скорости спинномозговой жидкости у людей-добровольцев и синусоидально колеблющиеся фантомные скорости существенно не различались между двумя используемыми методами МРТ [47]. Koerte et al. изучали две группы субъектов, визуализированных в двух разных помещениях с разным оборудованием. Они сообщили, что коэффициенты внутриклассовой корреляции (ICC) продемонстрировали высокую внутри- и межэксплуатационную надежность измерений объемного расхода PC-MRI, оставаясь независимыми от используемого оборудования и уровня квалификации оператора [48]. Хотя анатомические различия существуют между субъектами, это не помешало исследованиям на более крупных популяциях пациентов для описания возможных «нормальных» параметров оттока [49, 50].
Основываясь исключительно на субъективных восприятиях пациента, существуют ограничения в использовании результатов, сообщенных пациентом [51]. Любой аспект, влияющий на восприятие субъекта в их качестве жизни, может повлиять на результат любой оценки. Отсутствие специфичности результата при представлении симптомов, эмоций и инвалидности также ограничивает интерпретацию результатов [51].
Расходы на анализ изображений и МРТ не позволяют использовать контрольную группу, ограничивая любую обобщаемость этих результатов. Более большой размер выборки позволил бы сделать выводы на основе статистической мощности и уменьшенной ошибки типа I. Интерпретация любого значения в этих результатах, выявляя возможные тенденции, в лучшем случае остается предметом спекуляций. Большое неизвестное сохраняется в вероятности того, что эти изменения связаны с вмешательством или каким-либо другим эффектом, неизвестным исследователям. Эти результаты добавляют к совокупности знаний о ранее несопоставимых возможных гемодинамических и гидродинамических изменениях после вмешательства NUCCA, а также об изменениях в состоянии пациента с мигренью HRQoL, которые наблюдаются в этой когорте.
Значения собранных данных и анализов предоставляют информацию, необходимую для оценки статистически значимых размеров выборки субъекта в дальнейшем исследовании. Решенные процедурные задачи, связанные с проведением пилотного проекта, позволяют получить высоко уточненный протокол для успешного выполнения этой задачи.
В этом исследовании отсутствие надежного увеличения соответствия может быть понято логарифмическим и динамическим характером внутричерепного гемодинамического и гидродинамического течения, позволяя отдельным компонентам, содержащим соответствие, в то время как в целом этого не произошло. Эффективное вмешательство должно улучшить субъект, воспринимаемый боль и инвалидность, связанные с головной болью мигрени, как это измеряется этими инструментами HRQoL. Эти результаты исследования показывают, что вмешательство перестройки атласа может быть связано с уменьшением частоты мигрени, заметно улучшением качества жизни, что приводит к значительному снижению инвалидности, связанной с головной болью, как это наблюдается в этой когорте. Улучшение результатов HRQoL создает неоспоримый интерес для дальнейшего изучения, чтобы подтвердить эти результаты, особенно с большим пулом субъектов и группой плацебо.
Благодарности
Авторы признают доктора Ноама Алперина, Alperin Diagnostics, Inc., Miami, FL; Кэти Уотерс, координатор исследования и д-р Иордания Аусмус, координатор радиографии, клиника Британия, Калгари, AB; Сью Кертис, технолог МРТ, радиология Эллиота Фонга Уоллеса, Калгари, АБ; и Бренда Келли-Беслер, RN, координатор исследований, программа оценки и управления головной болью Калгари (CHAMP), Калгари, AB. Финансовую поддержку оказывает (1) Фонд Хехт, Ванкувер, Британская Колумбия; (2) Фонд Тао, Калгари, АБ; (3) Мемориальный фонд Ральфа Р. Григория (Канада), Калгари, АБ; и (4) Фонд верхних цервикальных исследований (UCRF), Миннеаполис, MN.
Сокращения
- ASC: Подвывицкий комплекс Atlas
- CHAMP: Программа оценки и управления головной болью Калгари
- CSF: Цереброспинальная жидкость
- GSA: анализатор силы тяжести
- HIT-6: Испытание на удар головной боли-6
- HRQoL: Качество жизни, связанное со здоровьем
- ICCI: Интракраниальный индекс соответствия
- ICVC: изменение внутричерепного объема
- IQR: межквартильный диапазон
- MIDAS: шкала оценки инвалидности мигрени
- MSQL: показатель качества жизни, характерный для мигрени
- MSQL-E: показатель качества жизни, обусловленный мигренью, - эмоциональный
- MSQL-P: показатель качества жизни, зависящий от мигрени, - физический
- MSQL-R: ограничение качества мигрени, ограничивающее мигрень
- NUCCA: Национальная ассоциация хиропрактики шейного отдела шейки матки
- PC-MRI: фазовая контрастность Магнитно-резонансная томография
- SLC: проверка на ногу на ногах
- VAS: визуальная аналоговая шкала.
Конфликт интересов
Авторы заявляют, что нет никаких финансовых или иных конкурирующих интересов в отношении публикации этого документа.
Вклад авторов
Х. Чарльз Вудфилд III задумал исследование, сыграл важную роль в его разработке, помог в координации и помог подготовить документ: введение, методы исследования, результаты, обсуждение и заключение. Д. Гордон Хасик проверил предметы для включения / исключения в исследование, при вмешательстве NUCCA и следил за всеми субъектами наблюдения. Он участвовал в разработке проекта и координации вопросов, помогая разрабатывать введение, методы NUCCA и обсуждение статьи. Вернер Дж. Беккер проверил темы включения / исключения в исследование, участвовал в разработке и координации исследований и помог подготовить документ: методы исследования, результаты и обсуждение и заключение. Марианна С. Роуз выполнила статистический анализ данных исследования и помогла подготовить документ: статистические методы, результаты и обсуждение. Джеймс Н. Скотт участвовал в исследовании дизайна, служил консультантом по визуализации, анализируя сканирование патологии и помогал разрабатывать документ: методы, результаты и обсуждение ПК-МРТ. Все авторы прочли и утвердили итоговый документ.
В заключение в тематическом исследовании, посвященном улучшению симптомов головной боли мигрени после пересадки позвонков атласа, было показано увеличение первичного результата, однако средние результаты исследования также не продемонстрировали статистической значимости. В целом, тематическое исследование показало, что у пациентов, получавших лечение пересадки позвонков в атласе, наблюдалось значительное улучшение симптомов со снижением периода головной боли. Информация, на которую ссылается Национальный центр биотехнологической информации (NCBI). Объем нашей информации ограничен хиропрактикой, а также травмами и состояниями позвоночника. Чтобы обсудить этот вопрос, пожалуйста, обращайтесь к доктору Хименесу или свяжитесь с нами по телефону 915-850-0900 .
Куратор д-р Алекс Хименес

Дополнительные темы: Шея
Боль в шее является обычной жалобой, которая может возникнуть из-за различных травм и / или состояний. Согласно статистике, телесные травмы и травмы хлыстовых травм являются одними из наиболее распространенных причин боли в области шеи среди населения в целом. Во время автокатастрофы внезапное воздействие этого инцидента может привести к тому, что голова и шея резко ударятся назад и вперед в любом направлении, что повредит сложные структуры, окружающие шейный отдел позвоночника. Травма сухожилий и связок, а также других тканей в области шеи может вызвать боль в шее и излучать симптомы во всем теле человека.

ВАЖНАЯ ТЕМА: ДОПОЛНИТЕЛЬНАЯ ЭКСТРА: Здорово!
ДРУГИЕ ВАЖНЫЕ ТЕМЫ: ДОПОЛНИТЕЛЬНО: спортивные травмы? | Винсент Гарсия | Пациент | El Paso, TX Chiropractor